Nitrosaminas em Medicamentos
Entenda o que são Nitrosaminas, mecanismo de toxicidade, limites e muito mais
O que são as nitrosaminas?
As nitrosaminas são moléculas que têm sido alvo constante de discussão perante as indústrias farmacêuticas e agências reguladoras, principalmente após 2018, quando foi relatada a primeira contaminação por moléculas de N-nitrosaminas potencialmente carcinogênicas em medicamentos. Mais recentemente, novas observações da presença de N-nitrosaminas em diferentes medicamentos levaram as autoridades regulatórias a solicitarem às empresas responsáveis pela comercialização de medicamentos humanos, avaliações completas de seus portfólios para ingredientes farmacêuticos ativos (IFAs) e produtos acabados (PA) que pudessem ter risco de contaminação por estas estruturas.
Interessantemente, esses compostos podem ser comumente encontrados na água, em alimentos, laticínios e vegetais e sua exposição dentro de limites seguros representa baixo risco de agravos à saúde. No entanto, a exposição acima de níveis aceitáveis e por longo período pode aumentar o risco de câncer.
Assim, a Agência Europeia de Medicamentos (EMA) definiu uma abordagem de três etapas para os titulares de autorizações de comercialização para a investigação e controle de nitrosaminas em medicamentos:
1) Realização da avaliação de risco para a presença de impurezas nitrosamina;
2) Caso identificado risco, testes confirmatórios são necessários para confirmar ou refutar a presença de nitrosaminas
3) Se necessário, mitigar a contaminação por nitrosaminas por meio de mudanças no processo de fabricação e implementação de uma estratégia de controle adequada.
Segundo a RDC 677 de 2022, que dispõe sobre avaliação de risco e controle de nitrosaminas potencialmente carcinogênicas em IFAs e medicamentos para uso humano, as empresas tem até junho de 2025 para avaliar todos os produtos do seu portifólio e os produtos inovadores também necessitam de avaliação quando submetidos os dossiês.
Como elas são formadas?
A formação de N-nitrosaminas depende de muitos fatores, principalmente a presença de compostos nitrogenados, de agentes nitrosantes e condições reacionárias propicias, como pH e temperatura, sendo que esses fatores podem estar presentes em qualquer etapa do processo. Ainda, dentro dos tipos de compostos nitrogenados, algumas classes são mais suscetíveis a nitrosação do que outras, como é o caso de aminas secundárias e terciarias.
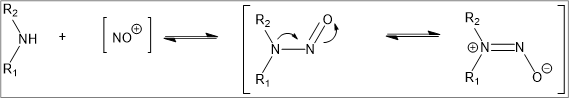
Figura 1: Reação de formação de derivados N-nitroso e suas formas de ressonância.
E elas são tóxicas?
Em relação a toxicidade, as nitrosaminas apresentam, principalmente, genotoxicidade devido a bioativação por CYP. Essa ativação resulta na formação de espécies diazonicas reativas ao DNA. Porém é importante frisar que nem toda a nitrosamina é carcinogênica/genotóxica e esta comprovação deve ser feita por estudos toxicológicos e análise de especialistas.
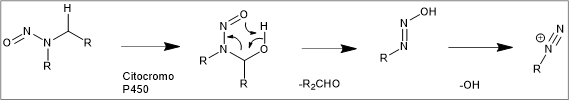
Figura 2: Formação do composto genotóxico.
Seus Limites Aceitáveis (Seguros)
É de conhecimento geral que, até certas concentrações, a ingestão de nitrosaminas não é preocupante. Dessa forma, é muito importante determinar os limites aceitáveis de ingestão (AI).
Dessa forma, para as nitrosamina conhecidas, como é o caso do NDMA, esse limite já é conhecido (NDMA = 96 ng/dia). Nesses casos os limites foram determinados a partir de estudos in vitro e in vivo ou ainda, a partir de read across com outras moléculas.
Já a determinação do AI para nitrosaminas que não conhecemos os limites, como é o caso das NDSRI (nitrosaminas derivadas do IFA), a abordagem CPCA (Carcinogenic Potency Categorization Approach), proposta pela EMA, pode ser aplicada. A predição é baseada na composição química e estrutural da nitrosamina a ser avaliada, em que são levados em consideração características estruturais ativantes ou desativantes, relacionados a um aumento ou diminuição da potência carcinogênica, respectivamente.
EMA x FDA
Mesmo que sejam agências regulatórias participantes do ICH (International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use) frequentemente encontramos divergências em suas análises, vide, alguns AI de Nitrosaminas e o valor de TCC (Threshold of Toxicological Concern) para estas estruturas que cada uma utiliza (26,5 µg/dia – FDA e 18 µg/dia – EMA). Isso ocorre porque cada agência possui o seu próprio entendimento sobre a realização de avaliações de riscos e diferença nas orientações regulamentares. Usualmente, utilizamos os valores do EMA por serem mais conservadores e pela Anvisa estar alinhada com as diretrizes desta agência.
Cálculo Cinético: Sólido x Líquido
Um ponto de bastante discussão sobre as avaliações de risco de nitrosaminas é a compreensão do risco de formação destas moléculas com base em informações cinéticas de reatividade entre aminas secundárias e nitritos.
A primeira etapa da avaliação de risco se baseia principalmente em estimar a formação de nitrosaminas a partir de uma estratégia que considera reações totais entre os compostos nitrogenados e agentes nitrosantes presentes durante a etapa de produção do medicamento. Durante essa avaliação, caso, as estimativas ultrapassem os limites, outras abordagens considerando mecanismos cinéticos e mecanísticos podem ser aplicados.
O mecanismo cinético mais aplicado e, primeiramente descrito, foi proposto por Ashworth et al e desenvolvido para soluções (nitrosação em solução). Entretanto, aplicá-lo para sólidos é um desafio, uma vez que reações em estado sólido não segue as mesmas regras (aspecto importante a ser considerando dentro do conceito de análise de risco e adaptações, mas isso é assunto para um outro post)
Dessa forma, uma das estratégias que poderia ser adotada é utilizar alguns dados conhecidos e aplicados em soluções (nitrosação) para sólidos. Contudo, ainda existem alguns desafios da extrapolação direta deste conceito com realidade, tendo chances até mesmo de ser apontado risco em situações que não há risco.
Felizmente, aqui na Spektra desenvolvemos adaptações/aproximações deste modelo que nos ajuda a trabalhar em casos como estes, considerando modelos como camada de umidade contígua e tamanho de partícula/interface superficial de degradação. Assim, nosso modelo permite que nossas estimativas sejam mais realistas.
Para saber mais
Agora que você já conhece tudo sobre nitrosaminas, novos questionamentos podem ter surgido. E para isso, convidamos vocês a assistir ao nosso podcast, onde abordamos mais sobre esse assunto e muito mais.
https://www.youtube.com/@PasteurlariaPodcast/playlists
Além disso, nos acompanhe por aqui pois traremos muita coisa para vocês ou deixe suas dúvidas nos comentários.
Bibliografia
Ashworth, I. A; Dirat, O.; Teasdale, A.; Whiting, M. Potential for the Formation of N‑Nitrosamines during the Manufacture of Active Pharmaceutical Ingredients: An Assessment of the Risk Posed by Trace Nitrite in Water. Org. Process Res. Dev. 2020, 24, 1629-1646.
EMA, Nitrosamine impurities, European Medicines Agency, Appendix 1: Acceptable intakes established for N-nitrosamines. Disponível em: <https://www.ema.europa.eu/en/human-regulatory/post-authorisation/referral-procedures/nitrosamine-impurities>.
EMA, Nitrosamine impurities, European Medicines Agency, disponível em: <https://www.ema.europa.eu/en/human-regulatory/post-authorisation/referral-procedures/nitrosamine-impurities>
ANVISA – Resolução da Diretoria Colegiada RDC vigente que Dispõe sobre avaliação de risco e controle de nitrosaminas potencialmente carcinogênicas em Insumos Farmacêuticos Ativos (IFA) e medicamentos de uso humano.
