QUALITY-BY-DESIGN na indústria farmacêutica
Entenda o que é o Quality by Design (QbD), como ele surgiu na indústria farmacêutica e quais são os principais elementos para sua aplicação.
O conceito de “Quality-by-Design” ou QbD é quase indissociável da figura de Joseph Juran, um dos grandes “gurus da Qualidade”. O QbD faz parte do tripé de Juran, que inclui também o Controle e a Melhoria de Qualidade.
A ideia básica é desenvolver um produto a partir de um planejamento cuidadoso desde sua concepção para garantir a qualidade no final do processo, estudando cada etapa, identificando pontos críticos e definindo estratégias para mitigar seus riscos. Ou seja, é projetar a qualidade pelo desenho (por isso, Quality by Design).
Essa ideia chegou ao mundo farmacêutico de forma mais evidente a partir do lançamento da iniciativa chamada de “Boas práticas de fabricação farmacêutica atuais para o Século XXI – Uma abordagem baseada em Risco” pela FDA. Logo em seguida, veio a publicação do Guia ICH Q8 – Pharmaceutical Development, que popularizou o QbD farmacêutico. Essa abordagem é baseada no conhecimento científico e na avaliação de riscos para desenvolver produtos com maior qualidade que garantam a eficácia e segurança aos pacientes.
Entre 2007 e 2008, foi desenvolvido um anexo ao guia ICH Q8 para incluir elementos importantes para auxiliar no desenvolvimento de processos e produtos farmacêuticos para gerar maior compreensão e, consequentemente, reduzir os riscos. Trazemos alguns desses elementos aqui:
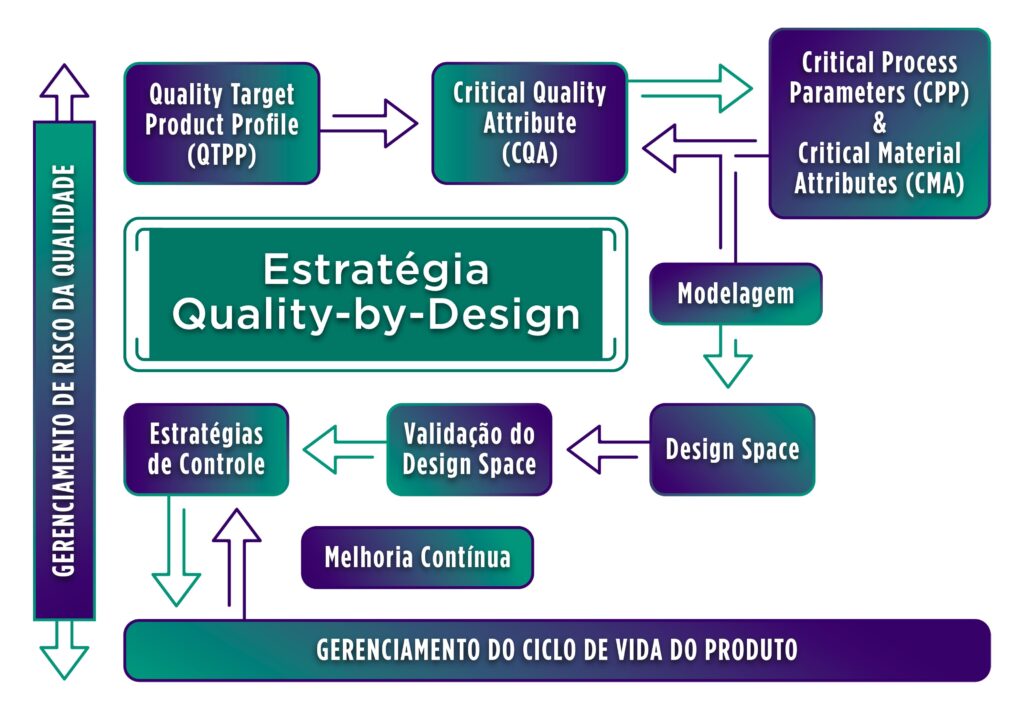
1 – Quality Target Product Profile (QTPP ou Perfil de Qualidade do Produto Alvo):
É a base que guiará o desenvolvimento do produto. Deve conter todas as informações relevantes considerando a qualidade desejada para o produto. Alguns exemplos podem incluir o uso pretendido no uso clínico, rota de administração, dosagem, pureza, esterilidade, dissolução etc.
2 – Critical Quality Attributes (CQA ou Atributos Críticos de Qualidade):
São as propriedades físicas, químicas, biológicas ou microbiológicas que devem estar dentro de limites ou intervalos apropriados para garantir que a qualidade adequada seja entregue.
3 – Avaliação de Risco (AR):
É usada para conectar os potenciais parâmetros críticos do processo (CPP) e/ou atributos críticos de material (CMA) ao CQA. A AR deve considerar conhecimentos prévios e justificar a escolha dos CPP e CMA para conduzir experimentos adicionais ou dispensarem de mais investigação. Importante ressaltar que a AR deve permear as decisões durante todo o ciclo de vida do produto.
4 – Design Space:
É a combinação multidimensional entre as variáveis de entrada (CPP e CMA) e suas potenciais interações que demonstrem o atendimento aos requisitos de qualidade de um ou mais CQA’s. Trabalhar dentro do Design Space não é considerado uma mudança. Para construí-lo, encoraja-se o uso de planejamento de experimentos (DoE), embora não seja uma etapa obrigatória, mas pode ajudar bastante para uma compreensão mais abrangente do processo.
5 – Estratégia de Controle:
Deve ser estabelecida para garantir a consistência na qualidade do produto. Os controles devem ser baseados na compreensão do produto, processo e formulações e devem incluir, no mínimo, o controle dos CPP e CMA, a partir da identificação de quais representam as principais fontes de variabilidade.
6 – Gerenciamento do Ciclo de Vida do Produto e Melhoria Contínua:
A performance do processo e a qualidade do produto devem ser monitoradas ao longo do ciclo de vida. Todos os elementos descritos anteriormente têm como objetivo dar o suporte fundamental para garantir o atendimento às especificações do produto, com o menor número de falhas possíveis. Além disso, o conhecimento gerado ao longo prazo pode ser usado para expandir, reduzir ou redefinir o Design Space, se necessário, trazendo melhorias e garantindo que o produto continue a entregar a qualidade, segurança e eficácia para a qual ele foi projetado.
Agora que você já conhece alguns dos conceitos básicos do QbD, é possível que novas dúvidas tenham surgido, como:
– Como posso aplicar o QbD no meu processo?
– Quais são as vantagens econômicas do QbD?
– E por que ele ainda não é tão difundido na indústria?
Então para saber mais, nos acompanhe por aqui pois traremos muita coisa para vocês ou deixe suas dúvidas nos comentários.

Ficou D+…Conteúdo de muito valor!!!