Impurezas mutagênicas: o que são e como atender aos requisitos do ICH M7
A segurança do paciente é um dos pilares fundamentais do desenvolvimento e da fabricação de medicamentos.
Nesse contexto, as impurezas mutagênicas ganharam grande destaque regulatório nos últimos anos, principalmente após a publicação do ICH M7, guideline que estabelece critérios rigorosos para a identificação, avaliação e controle dessas impurezas.
Falhas na gestão de impurezas mutagênicas podem resultar em riscos à saúde, questionamentos regulatórios, atrasos em registros e até na necessidade de ações corretivas em produtos já comercializados. Por isso, compreender o tema e aplicar corretamente os requisitos regulatórios é essencial para empresas farmacêuticas, farmoquímicas e de biotecnologia.
Neste artigo, você vai entender o que são impurezas mutagênicas, por que elas representam um risco crítico, o que o ICH M7 exige, como realizar uma avaliação de risco robusta e quais são os principais pontos de atenção exigidos por autoridades regulatórias como ANVISA, EMA e FDA.
O que são impurezas mutagênicas?
Impurezas mutagênicas são substâncias que apresentam potencial de causar alterações permanentes no material genético (DNA), podendo levar a efeitos adversos graves, como o desenvolvimento de câncer ao longo do tempo.
Elas fazem parte de um grupo maior chamado impurezas genotóxicas, mas nem toda impureza genotóxica é necessariamente mutagênica. As impurezas mutagênicas são aquelas para as quais existe evidência ou forte suspeita de capacidade de induzir mutações hereditárias.
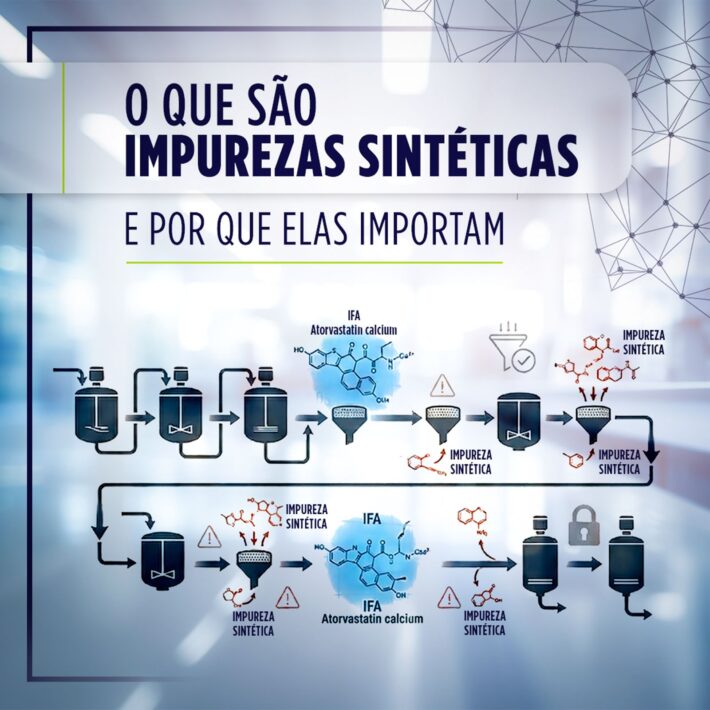
Essas impurezas podem surgir a partir de diferentes fontes, como:
- Reagentes e solventes utilizados na rota sintética
- Intermediários e subprodutos de processo
- Contaminantes provenientes de matérias-primas
- Produtos de degradação do fármaco ou do medicamento
Por esse motivo, a avaliação não se limita apenas ao produto final, mas envolve uma análise criteriosa de toda a rota de fabricação.
Por que as impurezas mutagênicas representam um risco crítico à saúde?
Diferentemente de outras impurezas, as impurezas mutagênicas podem causar efeitos adversos mesmo em níveis muito baixos de exposição, especialmente quando o medicamento é utilizado de forma crônica ou contínua.
O risco principal está associado ao potencial carcinogênico, uma vez que mutações no DNA podem se acumular ao longo do tempo. Por isso, a avaliação dessas impurezas considera não apenas a concentração no produto, mas também:
- Dose diária do medicamento
- Duração do tratamento
- População exposta
Esse racional levou à adoção do conceito de TTC (Threshold of Toxicological Concern), que estabelece um limite de exposição considerado aceitável para a maioria das impurezas mutagênicas, quando não há dados toxicológicos específicos disponíveis.
O que diz o ICH M7 sobre impurezas mutagênicas?
O ICH M7 – Assessment and Control of DNA Reactive (Mutagenic) Impurities foi desenvolvida com o objetivo de harmonizar a abordagem regulatória global para esse tema e garantir níveis adequados de segurança para os pacientes.
O guideline se aplica tanto a novos medicamentos quanto, em determinadas situações, a medicamentos já registrados, especialmente quando há mudanças de processo, novas impurezas identificadas ou atualizações de conhecimento científico.
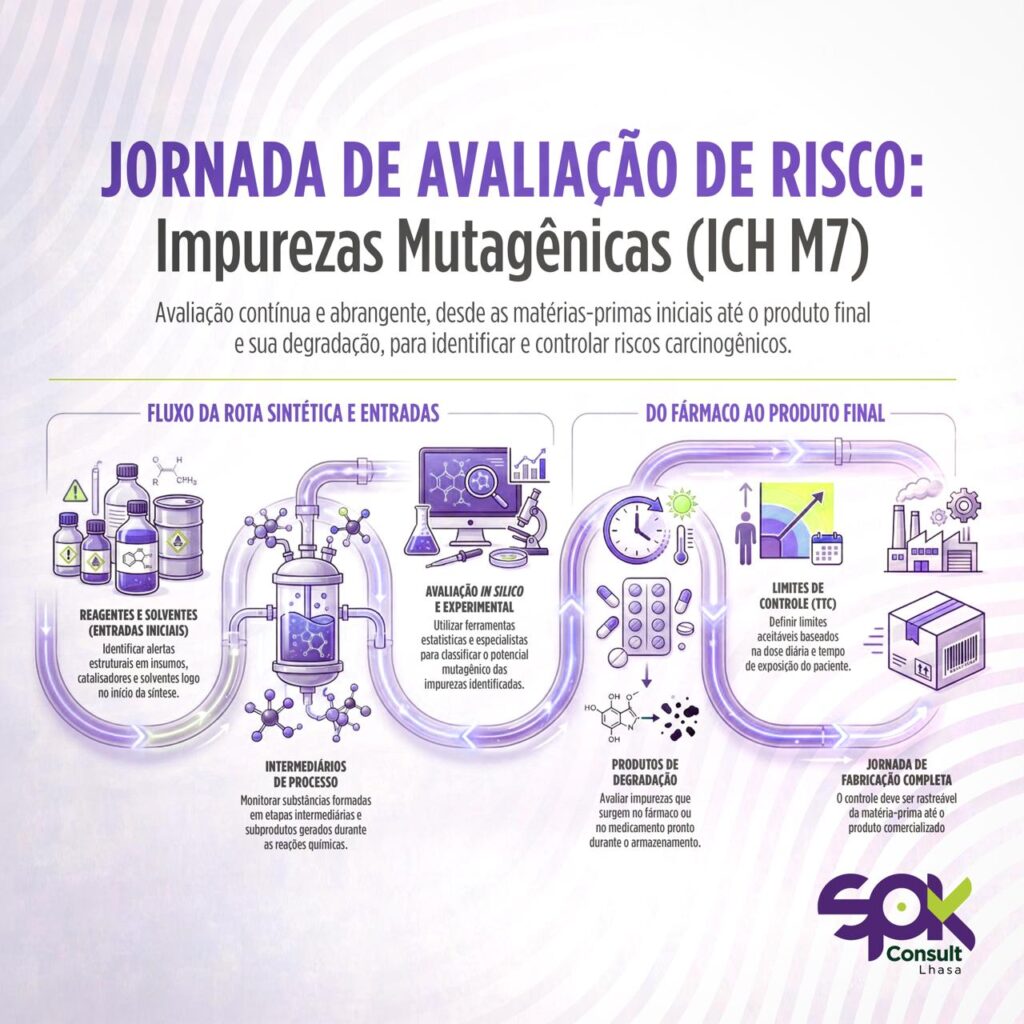
O ICH M7 propõe uma abordagem baseada em risco, que inclui:
- Identificação sistemática das impurezas potenciais
- Classificação quanto ao potencial mutagênico
- Definição de limites aceitáveis
- Estratégias de controle proporcionais ao risco
Classificação das impurezas segundo a ICH M7
O guideline classifica as impurezas em cinco classes:
- Classe 1: Impurezas sabidamente mutagênicas e carcinogênicas
- Classe 2: Impurezas conhecidas como mutagênicas, mas sem dados carcinogênicos
- Classe 3: Alerta estrutural para mutagenicidade, sem dados experimentais
- Classe 4: Impurezas com alerta estrutural relacionado ao ativo, mas considerados não mutagênicos;
- Classe 5: Impurezas sem alertas estruturais que demonstram ausência de mutagenicidade e carcinogenicidade.
Essa classificação orienta diretamente o nível de controle exigido.
Como é feita a avaliação de risco de impurezas mutagênicas?
A avaliação de risco de impurezas mutagênicas é um processo técnico e multidisciplinar, que deve ser bem documentado e justificável perante as autoridades regulatórias.
Identificação das potenciais impurezas
O primeiro passo consiste na análise detalhada da rota sintética do IFA, incluindo:
- Reagentes, catalisadores e solventes
- Intermediários isolados ou não
- Condições de reação
- Histórico de desvios e impurezas observadas
Também devem ser consideradas possíveis impurezas derivadas de degradação e impurezas provenientes de fornecedores.
Avaliação do potencial mutagênico
Uma vez identificadas, as impurezas são avaliadas quanto ao seu potencial mutagênico com base em:
- Dados experimentais disponíveis (ex: teste de Ames)
- Dados publicados na literatura científica
- Avaliação in silico por meio de ferramenta especialista e estatística conforme aceito pela ICH M7
Definição de limites aceitáveis
Quando uma impureza é classificada como potencialmente mutagênica, é necessário definir limites de controle apropriados, considerando:
- TTC (geralmente 1,5 µg/dia para exposições crônicas)
- Dose diária máxima do medicamento
- Duração do tratamento
- População-alvo
Esses limites devem ser tecnicamente justificados e refletidos nos métodos analíticos e nas estratégias de controle do processo.
Quais são as exigências da ANVISA, EMA e FDA?
As principais autoridades regulatórias, dentre elas, ANVISA, EMA e FDA, estão alinhadas aos princípios da ICH M7 e esperam que as empresas apresentem uma avaliação de risco formal e documentada sempre que aplicável.
Os principais pontos observados incluem:
- Justificativa clara sobre a aplicabilidade da ICH M7
- Avaliação científica das impurezas potenciais
- Critérios técnicos para definição de limites
- Estratégias de controle ao longo do ciclo de vida do produto
Durante submissões regulatórias, pós-registro ou inspeções, falhas nessa avaliação são frequentemente apontadas como deficiências relevantes.
Erros mais comuns na gestão de impurezas mutagênicas
Mesmo empresas experientes podem cometer equívocos nesse tema. Entre os erros mais frequentes estão:
- Assumir que a avaliação não é necessária sem justificativa formal
- Fazer uso inadequado de ferramentas in silico, sem interpretação crítica
- Definir limites sem racional científico consistente
- Falta de rastreabilidade da avaliação ao longo do ciclo de vida do produto
- Documentação insuficiente ou desatualizada
Evitar esses erros é fundamental para reduzir riscos regulatórios e proteger a segurança do paciente.
Como a Spektra apoia a gestão de impurezas mutagênicas
A Spektra Consultoria oferece suporte técnico especializado para empresas que precisam atender aos requisitos da ICH M7 de forma robusta e estratégica, incluindo:
- Avaliação de risco de impurezas mutagênicas conforme ICH M7
- Revisão crítica de dossiês regulatórios
- Definição de limites e estratégias de controle
- Suporte em interações com autoridades regulatórias
- Atualização de avaliações ao longo do ciclo de vida do produto
Nosso foco é garantir conformidade regulatória, segurança do paciente e eficiência nos processos regulatórios, reduzindo riscos e retrabalhos.
Perguntas frequentes sobre impurezas mutagênicas
O que caracteriza uma impureza mutagênica?
É uma impureza com potencial de causar alterações permanentes no DNA, podendo levar a efeitos carcinogênicos.
Toda impureza precisa ser avaliada segundo a ICH M7?
Nem todas, mas é necessário justificar tecnicamente a aplicabilidade ou não do guideline com base no processo e no produto.
A ICH M7 se aplica a medicamentos já registrados?
Sim, especialmente quando há mudanças de processo, novas impurezas identificadas ou solicitações de autoridades regulatórias.
O uso de in silico é obrigatório?
Sim, atualmente, o ICHM7 pede o uso de duas ferramentas complementares (estatística e especialista).
Impurezas mutagênicas se aplicam apenas a IFAs?
Não. A avaliação pode incluir impurezas presentes no produto acabado e impurezas formadas por degradação.
Conclusão
Uma gestão estratégica de impurezas mutagênicas fundamentada no ICH M7 entrega, de forma direta, às empresas:
- Conformidade rigorosa com as exigências da ANVISA, EMA e FDA;
- Segurança do paciente através da mitigação de riscos carcinogênicos;
- Agilidade na aprovação de registros e pós-registros, evitando atrasos;
- Emprego de racional científico robusto, utilizando conceitos como TTC e ferramentas in silico;
- Redução de retrabalhos e falhas críticas no ciclo de vida do produto.
Esses ganhos representam a garantia da integridade do medicamento e o sucesso absoluto nas submissões regulatórias.
Agora que você já entendeu a importância da gestão de impurezas mutagênicas, está pronto para elevar o patamar de segurança regulatória da sua empresa?
Entre em contato:
comercial@spektraconsultoria.com.br
www.spektracomercial.com.br