Análise de GAP de DMF para Fabricantes de Ativo: Por que é Essencial e Como Garantir Conformidade Regulatória
A indústria farmacêutica vive sob crescente pressão regulatória. Em um cenário marcado pela intensificação das inspeções e pela necessidade de rastreabilidade e transparência, o Drug Master File (DMF) tornou-se uma das principais ferramentas para assegurar a qualidade e a conformidade dos Insumos Farmacêuticos Ativos (IFAs).
Mas, apesar da sua importância, muitos fabricantes ainda enfrentam desafios para manter seus DMFs atualizados e alinhados às expectativas das autoridades sanitárias.
É aqui que entra a Análise de GAP de DMF, um serviço essencial para diagnosticar inconsistências, mitigar riscos e preparar fabricantes de IFA e detentores de registro para auditorias e submissões regulatórias.
Neste artigo, você entende por que essa análise é estratégica e como a Spektra Soluções Científicas apoia o setor com expertise técnica e visão regulatória.
O que é um DMF e por que ele é tão importante?
O Drug Master File é um documento técnico que descreve, em detalhes, a fabricação, o controle de qualidade e a gestão do ciclo de vida de um IFA ou material intermediário.
Ele serve como suporte regulatório para empresas que utilizam esse insumo na produção de medicamentos, preservando informações confidenciais do fabricante.
Sem um DMF bem estruturado e atualizado, empresas podem enfrentar:
- Exigências durante submissões;
- Riscos de desabastecimento devido à reprovação de fornecedores;
- Não conformidades em auditorias;
- Aumento de custos com retrabalho e correções de última hora.
O que é a Análise de GAP de DMF?
A Análise de GAP (GAP analysis) consiste em uma avaliação detalhada do DMF para identificar lacunas, inconsistências e pontos em desconformidade com guias regulatórios, tais como:
- ANVISA (RDC 359/2020 e correlatas)
- FDA (Guidances para DMFs Tipo II)
- ICH Q7, Q8, Q9 e Q11
- Requisitos específicos de mercados internacionais
O objetivo é estabelecer um diagnóstico claro do nível de aderência do fabricante e indicar ações corretivas priorizadas, garantindo previsibilidade e segurança nas submissões.
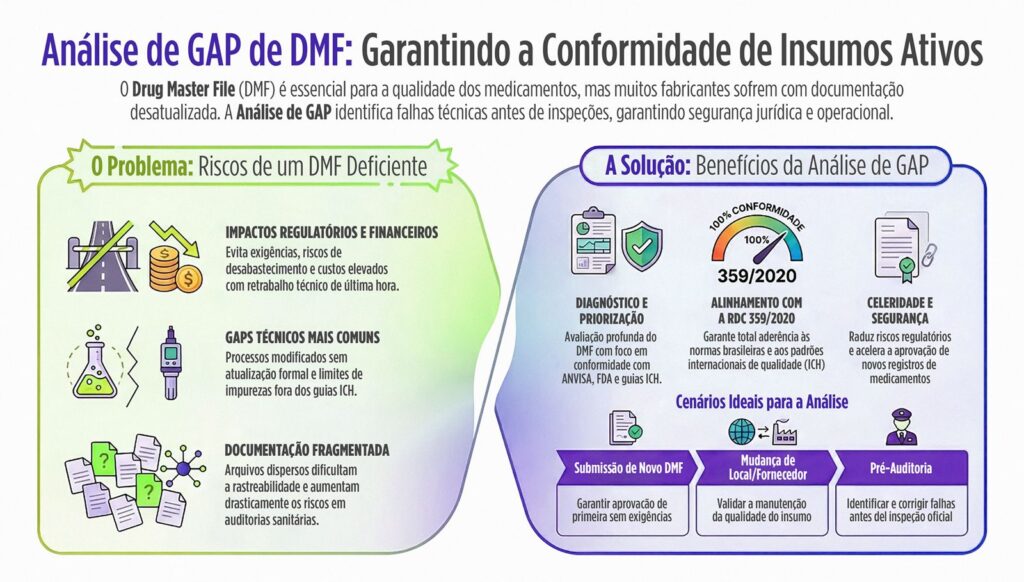
Principais problemas encontrados em DMFs
Durante as avaliações realizadas pela Spektra, alguns dos gaps mais frequentes incluem:
1. Falta de alinhamento entre etapas reais do processo e sua descrição no DMF
Processos modificados ao longo dos anos que nunca foram atualizados formalmente.
2. Especificações incompletas ou desalinhadas entre fabricante e cliente
Incluindo perfis de impurezas e limites fora dos guias ICH.
3. Dados insuficientes sobre variabilidade e controles críticos
Comumente associado à ausência de dados estatísticos consistentes.
4. Documentação fragmentada
Dificulta rastreabilidade e aumenta risco em auditorias.
5. Justificativas insuficientes para limite propostos
Incluindo impurezas mutagênicas e não mutagênicas.
Por que realizar uma Análise de GAP de DMF?
A análise representa um investimento estratégico, reduzindo riscos e acelerando submissões.
Entre os benefícios estão:
- Mais segurança em inspeções e auditorias;
- Redução do risco regulatório;
- Assertividade na comunicação com autoridades;
- Alinhamento com guias internacionais;
- Aumento da confiabilidade do fornecedor para clientes globais;
- Mais celeridade na condução de projetos de submissão regulatória, com redução de riscos
Como a Spektra Soluções Científicas apoia sua empresa
A Spektra conta com uma equipe altamente qualificada em qualidade, assuntos regulatórios e desenvolvimento analítico, oferecendo uma análise aprofundada e personalizada do seu DMF.
Nosso serviço inclui:
✔ Avaliação técnica do DMF;
✔ Identificação de gaps técnicos e regulatórios;
✔ Priorização de riscos;
✔ Recomendações detalhadas e acionáveis;
✔ Sugestão para correções.
Tudo isso com uma abordagem clara, estratégica e orientada a resultados.
Quando é o momento ideal para solicitar a Análise de GAP?
Recomendamos realizar a avaliação quando sua empresa estiver:
- Submetendo um novo DMF;
- Atualizando arquivos antigos;
- Mudando de fornecedor ou local de fabricação;
- Passando por auditorias regulatórias ou de clientes.
Conclusão
Manter um DMF robusto e alinhado às exigências regulatórias é essencial para garantir competitividade, qualidade e segurança regulatória.
Seja para entrada em novos mercados ou para evitar atrasos e retrabalhos, a Análise de GAP de DMF é um passo fundamental e a Spektra Soluções Científicas está ao seu lado para tornar esse processo mais simples, eficiente e seguro.
Quer avaliar o DMF do seu fabricante de ativo?
Fale com nossa equipe e receba um diagnóstico completo e personalizado.
Entre em contato:
comercial@spektraconsultoria.com.br
www.spektracomercial.com.br
Referências
- AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA (ANVISA). Resolução da Diretoria Colegiada – RDC nº 359, de 27 de março de 2020. Institui o Dossiê de Insumo Farmacêutico Ativo (DIFA). Diário Oficial da União: Brasília, 2020.
- AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA (ANVISA). Manual CADIFA – Procedimentos Administrativos. Brasília: Anvisa, 2025. Disponível em: <https://www.gov.br/anvisa/pt-br/centraisdeconteudo/publicacoes/medicamentos/publicacoes-de-insumos-farmaceuticos/manual-cadifa.pdf>.
- INTERNATIONAL COUNCIL FOR HARMONISATION OF TECHNICAL REQUIREMENTS FOR PHARMACEUTICALS FOR HUMAN USE (ICH). ICH Q7: Good Manufacturing Practice Guide for Active Pharmaceutical Ingredients. Geneva: ICH, 2016.
- INTERNATIONAL COUNCIL FOR HARMONISATION OF TECHNICAL REQUIREMENTS FOR PHARMACEUTICALS FOR HUMAN USE (ICH). ICH Q11: Development and Manufacture of Drug Substances. Geneva: ICH, 2012.
- INTERNATIONAL COUNCIL FOR HARMONISATION OF TECHNICAL REQUIREMENTS FOR PHARMACEUTICALS FOR HUMAN USE (ICH). ICH M7: Assessment and Control of DNA Reactive (Mutagenic) Impurities in Pharmaceuticals. Geneva: ICH, 2017.
- UNITED STATES. Food and Drug Administration (FDA). Guidance for Industry: Drug Master Files. Silver Spring: FDA, 2017. Disponível em: <https://www.fda.gov/regulatory-information/search-fda-guidance-documents/drug-master-files>.
- INTERNATIONAL COUNCIL FOR HARMONISATION OF TECHNICAL REQUIREMENTS FOR PHARMACEUTICALS FOR HUMAN USE (ICH). Organisation of the Common Technical Document for the Registration of Pharmaceuticals for Human Use – M4. Geneva: ICH.