O que são impurezas sintéticas e por que elas importam
Em síntese orgânica, Independentemente da escala, não existe reação “limpa“. Parece uma afirmação forte, mas na realidade se trata de uma consideração importante que deve ser feita ao se propor a rota sintética de compostos orgânicos bioativos. Ao longo de todo processo produtivo, a obtenção do princípio farmacêutico ativo (IFA) estará inevitavelmente associada à formação de impurezas sintéticas, provenientes de diferentes origens e mecanismos de reação.
Nesse contexto, conhecer as impurezas intrínsecas dos processos produtivos não se traduz apenas em conformidade regulatória, mas acima de tudo, segurança ao paciente e garantia de qualidade do medicamento. Compreender a origem dessas impurezas permite mitigar sua formação, evitar seu carreamento ao longo da síntese, e definir estratégias adequadas de monitoramento e controle quando essas impurezas alcançam o IFA ou medicamento acabado.
Mas afinal, o que são impurezas sintéticas?
Impurezas sintéticas podem ser definidas como todo e qualquer composto orgânico presente no IFA ou no medicamento acabado que possua estrutura química diferente do fármaco (excluindo-se os excipientes), e que se origine direta ou indiretamente do processo de síntese.
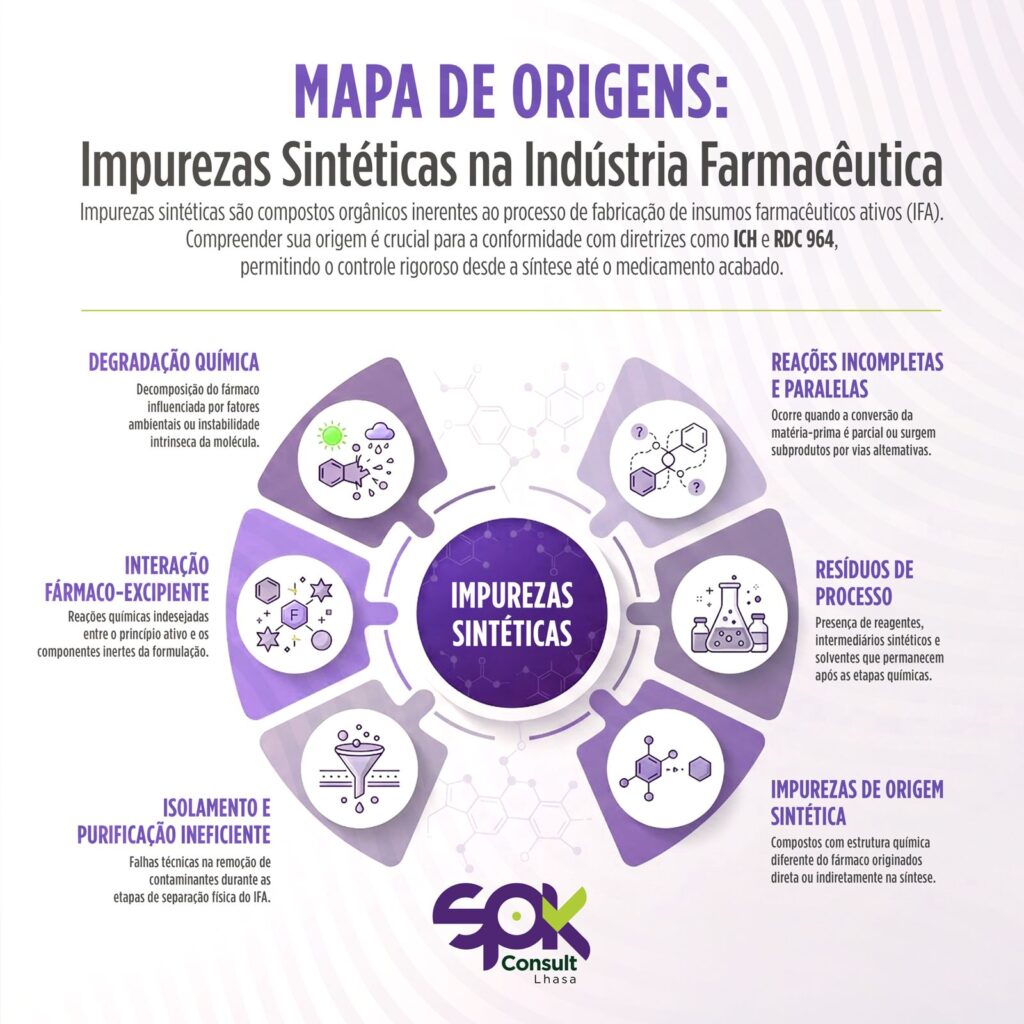
Essas impurezas podem surgir a partir de diferentes mecanismos, incluindo:
- reações incompletas;
- reações paralelas ou concorrentes;
- ineficiência nos processos de isolamento e purificação;
- interações fármaco‑excipiente;
- reações de degradação química.
Além disso, resíduos de reagentes, intermediários sintéticos e solventes também são classificados, do ponto de vista regulatório, como impurezas relacionadas ao processo. Assim, as impurezas sintéticas devem ser entendidas como parte inerente do processo produtivo e tratadas como um elemento integrante e crítico do desenvolvimento farmacêutico.
Impurezas sintéticas e requisitos regulatórios
As expectativas regulatórias relacionadas às impurezas sintéticas são amplamente fundamentadas em diretrizes internacionais harmonizadas. Entre os principais referenciais estão as diretrizes ICH Q3A e ICH Q3B, que estabelecem os limites de identificação, qualificação e notificação de impurezas orgânicas em IFAs e produtos farmacêuticos acabados, respectivamente, e o ICH Q3C, voltado ao controle de solventes residuais com base em avaliação toxicológica. Para impurezas com potencial mutagênico, o ICH M7 introduz uma abordagem ainda mais rigorosa, baseada em avaliação de risco, conceitos como TTC (Threshold of Toxicological Concern) e uso de ferramentas preditivas.
No contexto brasileiro, esses princípios foram consolidados e reforçados por meio da RDC nº 964/2025, que define critérios para qualificação de impurezas e produtos de degradação, estabelecendo quando são exigidos estudos adicionais de segurança com base em exposição, toxicidade e relevância clínica. A RDC 964 reforça a adoção de uma abordagem científica e baseada em risco, em alinhamento direto com as diretrizes ICH, e estabelece expectativas claras quanto à robustez técnica das justificativas apresentadas.
Conclusão
Agências reguladoras como ANVISA, FDA e EMA esperam que esses princípios sejam incorporados de forma consistente aos dossiês técnicos, tanto em registros iniciais quanto em atividades de pós‑registro. Nesse cenário, o dossiê de impurezas assume papel central, funcionando como um documento integrador que conecta processo produtivo, dados analíticos, avaliação toxicológica e estratégia de controle ao longo de todo o ciclo de vida do medicamento
Compreender a origem das impurezas sintéticas é, portanto, um requisito essencial para garantir a qualidade do medicamento, a segurança do paciente e a conformidade regulatória. Diretrizes internacionais e normas nacionais reforçam a necessidade de uma abordagem científica, integrada e baseada em risco, que fortalece a robustez dos processos, reduz incertezas regulatórias e sustenta a tomada de decisões ao longo de todo o ciclo de vida do medicamento.
Quer garantir a correta qualificação das impurezas sintéticas do seu IFA?
Fale com nossa equipe e receba um diagnóstico completo e personalizado baseado nas diretrizes ICH e normas nacionais.
Entre em contato:
comercial@spektraconsultoria.com.br
Referências
ICH Q3A (R2): Impurities in new drug substances. Geneva: ICH, 2006.
ICH Q3B (R2): Impurities in new drug products. Geneva: ICH, 2006.
ICH Q3C (R8): Impurities: guideline for residual solvents. Geneva: ICH, 2021.
ICH M7 (R2): Assessment and control of DNA reactive (mutagenic) impurities in pharmaceuticals. Geneva: ICH, 2023.
BRASIL. Agência Nacional de Vigilância Sanitária (ANVISA).
Resolução da Diretoria Colegiada – RDC nº 964, de 20 de fevereiro de 2025. Dispõe sobre os critérios para qualificação de impurezas e produtos de degradação em medicamentos. Diário Oficial da União: Brasília, 21 fev. 2025.


